Propriedades Coligativas Exemplos Do Dia A Dia – Descubra o fascinante mundo das Propriedades Coligativas: Exemplos Do Dia A Dia! Aqui, mergulharemos nos efeitos práticos dessas propriedades em nossas vidas, desvendando seus mistérios e aplicações de forma clara e envolvente.
Essas propriedades influenciam desde a fervura da água até o congelamento do sorvete, tornando-se essenciais para entender diversos fenômenos cotidianos.
Pressão de Vapor

As propriedades coligativas afetam a pressão de vapor de uma solução, o que se refere à tendência das moléculas de um líquido escaparem para a fase gasosa. Soluções com propriedades coligativas mais altas têm pressões de vapor mais baixas do que os solventes puros.Uma
aplicação comum desse efeito é a adição de sal à água para aumentar seu ponto de ebulição. Ao aumentar a concentração de soluto na água, sua pressão de vapor diminui, exigindo uma temperatura mais alta para atingir a pressão de vapor da atmosfera e ferver.
Exemplos do Dia a Dia
- A adição de anticongelante ao radiador de um carro reduz seu ponto de congelamento e aumenta seu ponto de ebulição. Isso ocorre porque o anticongelante diminui a pressão de vapor da água, impedindo que ela congele em temperaturas mais baixas e evapore em temperaturas mais altas.
- A adição de açúcar à água para fazer xarope reduz sua pressão de vapor, aumentando seu ponto de ebulição e tornando-o mais espesso.
Ponto de Ebulição: Propriedades Coligativas Exemplos Do Dia A Dia

O ponto de ebulição é a temperatura na qual a pressão de vapor de um líquido é igual à pressão externa. A adição de um soluto não volátil a um solvente aumenta o ponto de ebulição da solução. Isso ocorre porque as moléculas do soluto competem com as moléculas do solvente por espaço na superfície do líquido, dificultando a evaporação das moléculas do solvente.
A elevação do ponto de ebulição é uma propriedade coligativa, o que significa que depende apenas da concentração do soluto e não da sua natureza. A elevação do ponto de ebulição é proporcional à molalidade da solução, que é definida como o número de moles de soluto por quilograma de solvente.
Exemplos de Elevação do Ponto de Ebulição
- A adição de sal à água aumenta o ponto de ebulição da solução. Esta propriedade é usada em cozinhar para ferver alimentos mais rapidamente.
- O anticongelante é adicionado aos radiadores dos carros para evitar que a água congele em temperaturas abaixo de zero. O anticongelante aumenta o ponto de ebulição da água, evitando que ela ferva e danifique o motor.
Ponto de Congelamento

As propriedades coligativas também afetam o ponto de congelamento das soluções. Quando uma substância é dissolvida em um solvente, o ponto de congelamento da solução diminui em relação ao solvente puro.
Isso ocorre porque as partículas dissolvidas interferem na formação de cristais de solvente, dificultando o congelamento da solução. Quanto maior a concentração da solução, maior será a diminuição do ponto de congelamento.
Situações Cotidianas
- Sal de cozinha para derreter gelo:O sal de cozinha é um soluto que diminui o ponto de congelamento da água. Quando o sal é espalhado sobre o gelo, ele cria uma solução salina que derrete o gelo a uma temperatura mais baixa do que a água pura congelaria.
- Anticongelante em carros:O anticongelante é um líquido que contém solutos que diminuem o ponto de congelamento da água. Ele é adicionado à água do radiador dos carros para evitar que congele em temperaturas baixas, o que poderia danificar o motor.
- Refrigeradores e congeladores:Os refrigeradores e congeladores usam um sistema de refrigeração que envolve a evaporação de um líquido refrigerante. A evaporação do refrigerante diminui a temperatura dentro do aparelho, criando um ambiente mais frio que o ponto de congelamento da água. Isso permite que os alimentos sejam armazenados em temperaturas abaixo de zero, sem congelar.
Pressão Osmótica

A pressão osmótica é uma propriedade coligativa que mede a tendência de um solvente se mover através de uma membrana semipermeável de uma solução menos concentrada para uma solução mais concentrada.
As propriedades coligativas afetam a pressão osmótica porque elas determinam a concentração de partículas em uma solução. Quanto maior a concentração de partículas, maior a pressão osmótica.
Exemplos Comuns de Pressão Osmótica
Aqui está uma tabela com alguns exemplos comuns de pressão osmótica em diferentes contextos:
| Contexto | Exemplo |
|---|---|
| Biologia | A pressão osmótica é responsável pelo movimento da água para dentro e para fora das células. |
| Medicina | A pressão osmótica é usada para tratar condições como desidratação e choque. |
| Ciência dos Materiais | A pressão osmótica é usada para criar materiais com propriedades específicas. |
Aplicação em Indústrias
As propriedades coligativas são amplamente utilizadas em diversos setores industriais, pois permitem controlar e prever o comportamento de soluções e misturas em diversas aplicações.
Indústria Alimentícia
- Controle da pressão osmótica:A pressão osmótica é utilizada para preservar alimentos por meio de processos como osmose reversa e desidratação. Esses processos removem o excesso de água, inibindo o crescimento de microrganismos e prolongando a vida útil dos alimentos.
- Determinação do ponto de congelamento:O ponto de congelamento é usado para controlar a qualidade de sucos, refrigerantes e outros produtos alimentícios. O ponto de congelamento mais baixo indica uma maior concentração de solutos, o que pode afetar o sabor e a textura do produto.
Indústria Farmacêutica
- Controle da pressão de vapor:A pressão de vapor é usada para controlar a evaporação e sublimação de medicamentos. Isso é importante para garantir a estabilidade e eficácia dos medicamentos durante o armazenamento e transporte.
- Determinação do ponto de ebulição:O ponto de ebulição é usado para controlar a temperatura de ebulição de soluções, o que é essencial em processos de destilação e purificação de medicamentos.
Indústria Química
- Separação de misturas:As propriedades coligativas são usadas para separar misturas com base em suas diferenças de pressão de vapor, ponto de ebulição ou ponto de congelamento. Isso é aplicado em processos como destilação fracionada e cristalização.
- Controle da reatividade:As propriedades coligativas são usadas para controlar a reatividade de soluções alterando sua concentração ou composição. Isso é importante em reações químicas para controlar a taxa de reação e o rendimento do produto.
Indústria de Petróleo, Propriedades Coligativas Exemplos Do Dia A Dia
- Controle do ponto de congelamento:O ponto de congelamento é usado para controlar a temperatura de congelamento do petróleo bruto durante o transporte e armazenamento. Isso evita a formação de cristais de gelo, que podem danificar os equipamentos e obstruir os oleodutos.
- Determinação da pressão de vapor:A pressão de vapor é usada para controlar a evaporação de componentes voláteis do petróleo bruto durante o armazenamento e transporte. Isso reduz as perdas e garante a segurança do processo.
Concluindo, as Propriedades Coligativas são ferramentas valiosas para compreender e manipular soluções em diversos campos. Seja na cozinha, na indústria ou na pesquisa científica, essas propriedades desempenham um papel crucial, tornando nossa vida mais fácil e abrindo novas possibilidades.
Question Bank
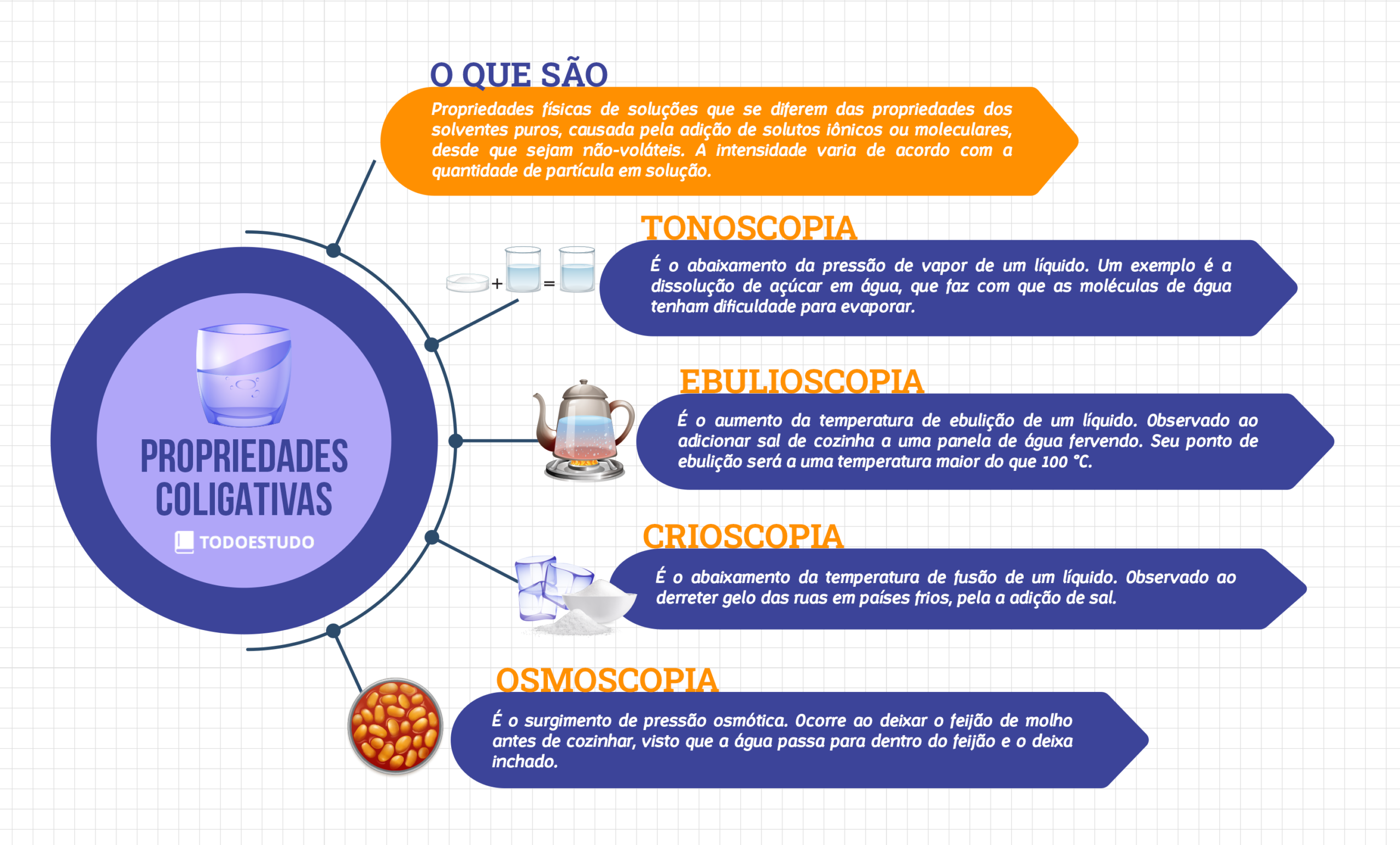
O que são Propriedades Coligativas?
São propriedades de soluções que dependem apenas da concentração de soluto, não de sua natureza química.
Como as Propriedades Coligativas afetam o Ponto de Ebulição?
Elas elevam o ponto de ebulição, ou seja, a solução ferve em uma temperatura mais alta que o solvente puro.

